Ədəbiyyatın son icmalı: oktyabr 2016. || Məqalənin son yenilənmə tarixi: oktyabr 2016.
GİRİŞ.
Xəstəxanadaxili pnevmoniya (XDP) xəstəxanaya yerləşdirildikdən 48 saat sonra qazanılan və müraciət vaxtı inkubasiya halında olmayan kəskin aşağı tənəffüs yolları infeksiyasıdır. [1] XDP-ın spektri endotraxeyal intubasiyadan 48 saat sonra baş verən ventilyasiya əlaqəli pnevmoniyadan (VƏP) fərqlidir. Dərman Assosasiyalı nevmoniya (DAP), İnfeksion Xəstəliklər Cəmiyyəti və Amerika Torakal Cəmiyyəti tərəfindən XDPvə VƏP -lər üçün tərtib edilmiş təlimatlarda artıq kliniki hal sayılmır.
Etiologiya
Bakteriyalar bir çox XDP xəstəlik hadisəsinə və ventilyasiya ilə əlaqəli pnevmoniyaya səbəb olur, o cümlədən Pseudomonas aeruginosa, Escherichia coli, Klebsiella pneumoniae və Acinetobacter növləri. Metisillinə həssas Stafilokokk aureus (MSSA) əlavə olaraq, həm xəstəxanadaxili həm də xəstəxanadankənar MRSA ştammları, XDP xəstəlik hadisələrinin artmasına səbəb o Orofaringeal mikroorganizmlər (viridans qrup streptokoklar, koaqulyaz-mənfi stafilokoklar, Neisseria növləri və Korinebakterium növləri) və anaerob orqanizmlər XDP-ın nadir səbəbləridir. Mikrobəleyhinə preparatlar qəbul etmiş və ya xəstəxanadankənar təcili yardım səhiyyə müəssisəsinə müraciət etmiş xəstələr əksər dərmanlara davamlı (DDP) patogenləri ilə yoluxmuş ola bilər və bu patogenlərə görə (məs. P aeruginosa və MRSA) XDP riski daşıyırlar.[3] DDP patogenləri intensiv terapiya şöbələrində də ola bilər; bunun üçün də intensiv terapiya şöbələrinin aktiv müşahidəsi tövsiyyə edilir. [3] Palatadakı xəstələrdə XDP Streptokokk pnevmoniyae və Legionella növləri kimi xəstəxanadaxili olaraq az tanınan patogenlərə görə ola bilər.[14] Legionella pnevmofila görə XDP təsadüfidir, ancaq su təchizatı mənbəyi yoluxduqda və ya davam edən inşaat işləri olduqda, seroqrup 1 ilə daha çox yayılır. [15] Virus və göbələk mənşəli etiologiyalar da nadirdir, ancaq hər biri üçün insident göstəricisi yüksək ola bilər (məs. əgər qrup alovlaması baş versə və yaxud immun sistemi zəifləmiş xəstələrə hava təmin edən kanalda Aspergillus olsa).[16] [17]
Patofiziologiya
Bakteriyaların alveollara daxil olmasının əsas yolu,orofaringeal patogenlərin mikroaspirasiyası və endotraxeal boruya bakteriyalı seliyin sızmasıdır.[18] Digər yoluxma yollarına makroaspirasiya (məs. qusmanın), inhalyasiya, yoluxmuş venadaxili kateterlərdən hematogenoz yayılma, birbaşa innokulyasiya (məs. torasentez) və mədə-bağırsaq traktından translokasiya aiddir. [19] Təsvir edilən yoluxma yollarına xəstələri təhrik edən vacib faktorlara, xəstələrin əsas xəstəliyinin ağırlıq dərəcəsi, əvvəlki cərrahiyyə əməliyyatı, mikrobəleyhinə preparatlar, digər dərmanlar, invaziv tənəffüs cihazları və aparatları aiddir. [20] XDP üçün patogen mənbələrinə tibbi avadanlıqlar(endotraxeya borusunda yoluxmuş biotəbəqə ), ətraf mühit (hava, su, avadanlıq), habelə mikroorqanizmlərin xəstədən xəstəyə tibb işçiləri vasitəsi ilə ötürülməsi (pis əl gigiyenası) daxildir. [21] [22] Son olaraq sinus boşluqları, XDP-a yol açan, dərmanla əlaqəli patogenlərin rezervuarı ola bilər. [23]
Bakterial həssaslıq xəstəliyin inkişafında əhəmiyyətli cəhətdir. [24] XDP xəstələrində onların endogen florası yuxarı tənəffüs yollarının yoluxması üçün mənbə təşkil edir. Qram mənfi orqanizmlərə meyillilik ola bilər, çünki tüpürcəkdə artmış proteaz maddəsi var və ağız hüceyrə səthlərində fibronektin itkisinin baş verməsi səbəbindən adgeziyanın güclənməsi və tənəffüs yollarının selikli qişasının qram mənfi bakteriyalar ilə kolonizasiyası baş verir. Adətən, selikli qişa hüceyrələri qram müsbət bakteriyaların adgeziyasına qarşı fibronektinlə örtülmüş olur.[24]
Təsnifat
Xəstəxanadaxili pnevmoniya (XDP).
• Xəstəxanaya müraciətdən 48 saat sonra qazanılmış kəskin aşağı tənəffüs yolları infeksiyası.
Ventilyasiya əlaqəli pnevmoniya (VƏP)
• Endotraxeya intubasiyasından sonrakı >48 -72 saat ərzində yaranan pnevmoniya.
PROFİLAKTİKA TƏDBİRLƏRİ.
Birincili profilaktika
Profilaktikada diqqət əsasən infeksiyaya nəzarət, müəyəyn prosedurlardan/təsirlərdən yayınma və müəyən idarəetmə strategiyalarina yönəldilməlidir.
İnfeksiyaya nəzarət
• Əl gigiyenası bir tibb işçisinin edə biləcəyi ən vacib ilkin profilaktika strategiyasıdır və bu Acinetobacter kimi XDP-a səbəb olan əksər dərmanlara davamlı (DDP) patogenlərin ötürülməsinin qarşısını alır. [30] [36] [37]
• Digər infeksiyaya nəzarət tədbirləri, o cümlədən işçilərin təlimi və təcrid edilməsi, DDP -lər ilə çarpaz yoluxma hallarını azaltmaq üçün müntəzəm olaraq görülməlidir.[3]
• İTŞ-də infeksiyalara nəzarət zamanı bir neçə iş icra edilir: endemik və yeni DDP-lər təyin edilir, infeksiya nəzarəti üçün vaxtlı vaxtında məlumat hazırlanır və ehtimal edilən XDP xəstələrində müvafiq mikrobəleyhinə müalicə istiqamətləndirilir. [3]
• İnfeksiyaya nəzarət və profilaktika tədbirləri olmasa ,xəstə xəstəxanaya infeksiyasız qəbul edilib sonra ciddi xəstələnmə göstəricisi ilə buraxıla bilər, və yaxud da buraxılmadan əvvəl ölə bilər. Proses, orqanizmin DDP tərəfindən kolonizasiyası ilə başlayır, daha sonra steril toxumaları patogenlər zəbt edir (məs. ağciyər, qan) və xəstəliklə (məs. XDP, bakteriemiya) və hətta ölümlə nəticələnir.
Yayınılması vacib olan təsirlər
• Lazım olmayan mikrobəleyhinə dərman istifadəsi, davamlı mikrobəleyhinə preparatların iTŞ-lərdə qalmasının və xəstələri yoluxdurmasının qarşısını alır. Lazım olmayan intubasiyanın qarşısı qeyri-invaziv müsbət təzyiq ventilyasiyası ilə alına bilər, tənəffüs pozğunluğu olan və tənəffüs çatışmazlığı yaşamayan, uzun müddətli köməyə ehtiyacı olmayan xəstələr üçün aralıq oksigenləşdirmə və ventilyasiya üsuludur. 16 təsadüfi sınaqlar üzərində meta-analiz aparılıb və yaxşılaşmış nəticələr tapılıb: azalmış ventilyasiya əsaslı pnevmoniya (VƏP) nisbəti, daha aşağı ölüm göstəricisi, daha qısa İTŞ qalma müddəti və daha qısa xəstəxanada qalma müddəti. [38] Lazım olmayan sedasiyanın qarşısını almaq 'tənəffüs yollarını qorumaq' üçun xəstələrin intubasiyasının qarşısını alır. Sedativlərin dayandırılması intubasiya müddətini qısaldır və bunun üçün də VƏP azalır. [39] Sedativ fasilə verilməsi üçün daha çox İTŞ işçiləri tələb edir və bu təcrübəni protokollara əlavə etməzdən əvvəl resursların mövcudluğu yoxlanılmalıdır. [CDC: National Healthcare Safety Network] [CDC: Healthcare Infection Control Practices Advisory Committee]
Xüsusi menecment strategiyaları
• Müntəzəm sxem dəyişmənin lazım olmağıdı haqqında məlumat olmasına baxmayaraq, həftəlik olaraq ventilyasiya dövrlərini dəyişmək baxım standartına çevrilib. [40] [41] Başlıq təzyiqi >20 sm H2O olaraq saxlanılmalıdır. İTŞ-də xlorheksidinlə oral gigiyena yayılmış təcrübədir.[42] [43]
• Xəstəyə 45° yarım-uzanmış vəziyyətin verilməsi VƏP hallarını ciddi surətdə azaltdığı müşahidə edilib. [44] Endotraxeal borular, bakterial kolonizasiya və biotəbəqə yaranmasını dizayn xüsusiyyətləri ilə və ya aspirat təhlükəsi olan subqlottik sekresiyaları sovurma yolu ilə, VƏP-in qarşısını ala bilər.[45] [46] Xüsusi endotraxeya borularından istifadə edilərək aparılan tədqiqatlar erkən başlayan VƏP göstəricisində və digər nəticələrdə ciddi azaltma olduğunu göstərir. [39] [45] [46] [47] ] Ventilyasiya dövr kolonizasiyasını azaldan passiv nəmləndiricilər və ya istilik-nəmlilik mübadilə avadanlıqlarının, ardıcıl surətdə VƏP göstəricisini azaltdığı müşahidə edilməyib. Probiotiklərlə əlaqəli 5 təsadüfi nəzarət sınaqlarına görə, onların istifadəsi azalmış VƏP nisbəti və İTŞ-də qalma müddəti ilə əlaqəlidir, ancaq İTŞ və ya xəstəxanadaxili ölüm göstəricisi və ya mexaniki ventilyasiya müddətində dəyişiklik yoxdur. [48] Lakin həzm sisteminin selektiv zərərsizləşdirilməsindən getdikcə daha çox istifadə olunur.[49] Venadaxili mikrobəleyhinə preparatların qısa müddətli istifadəsindən əlavə olaraq rezistent qram-mənfi bakteriyaların oxalmasının qarşısını almaq üçün ağız-udlaq və mədəyə yerli mikrobəleyhinə preparatlar tətbiq edilir və beləliklə xəstəxanadaxili infeksiyaların qarşısı alınır.
• Stress mənşəli xoranın profilaktikası üçün ən yaxşı maddə məlum deyil (sukralfat, H2-reseptor antaqonistlərə qarşı), ancaq 1998-ci ildə aparılan ən geniş tədqiqatda sukralfata üstünlük verilib. [23] Digər bir tərəfdən, 11 tədqiqatda aparılan və hansı maddənin daha yaxşı olduğunu müəyyənləşdirən meta analizə görə, H2 reseptor antaqonistləri verilən xəstələrdə daha yüksək qastrik kolonizasiya və VƏP göstəriciləri var. [50] Hər iki maddə açıq qastrik qanaxmanı bərabər qaydada müalicə edib.
Bu profilaktik fəaliyyətlərin əksəriyyəti, daha əhatəli formada təcrübə edilməsi üçün 'paketlər' halında tibbi işçilər üçün toplanılıb. Bu cür paketlər, fərdi baxım azlığı və müəyyən xəstələr üçün təhlükəli sayılan mümkün tapşırıqlara görə təndiq edilir. Hollandiyada aparılan potensial tədqiqatda sepsis paket proqramında iştirak edən 52 İTŞ ilə iştirak etməyən 30 İTŞ-ki ölüm göstəricisi qarşılaşdırılıb. [51] Tədqiqatda aşkarlanıb ki, sepsis paket proqramında iştirak edən İŞT-də 3.5 il ərzində xəstəxanadaxili ölüm göstəricisi (aylıq tənzimlənmiş nisbət = 0.992 [0.986-0.997]) 5.8% tənzimlənmiş mütləq nisbətdə azalıb.
İkincili profilaktika
Qrip vaksini, xəstəlik alovlanması olan müəssisədə olanlar və ya yerli kriteriyalara uyğun gələnlər üçün nəzərə alınır. Qripdən sonra bakterial pnevmoniya baş verə bilər, onun üçün immunizasiya əhəmiyyətlidir. Əgər qrip diaqnozu qoyularsa, neyraminidaza inhibitorları ilə erkən virus əleyhinə müalicə qripin və pnevmoniyanın tibbi müəssisələr daxilində yayılmasının qarşısını alır. [3] [16] Hər hansı bir əks-göstəriş olmadıqda, bütün tibb işçiləri qripə qarşı vaksinasiya olunmalıdırlar.[112]
Pnevmokok polisaxxarid vaksini (PPSV23) xəstəxanaya yerləşdirilmiş xəstələr üçün xüsusi olaraq göstərilməyib, ancaq yanaşı xəstəlikləri olan Streptokokk pnevmoniyaeolan xəstələrdə infeksiyaların qarşısını almağa kömək edə bilər. Pnevmokok vaksinində 23 antigendən saflaşdırılmış kapsulalı polisaxxaridlər var və 65 yaşdan böyük və yanaşı xəstəlikləri olan xəstələr üçün nəzərdə tutulub. [113] S pnevmoniyae üçün vaksik, pnevmokokk konyuqat vaksini (PCV13) yaşı 50-dən böyük olan xəstələr üçün nəzərdə tutulub.
MƏRHƏLƏLİ DİAQNOSTİK YANAŞMA.
XDP diaqnozu qeyri-adi vizuallaşdırma üsulu və 3 kliniki xüsusiyyətlərdən 2-ni tələb edir: hərarət >38°C (100.4°F), leykositoz və ya leykopeniya və yaxud irinli sekresiyalar. [1] Digər simptomlara öskürək, döş qəfəsində ağrı və ya əzginlik daxildir. Kliniki müayinə əlamətlərinə döş qəfəsinin qeyri-simmetrik genişlənməsi, azalmış rezonans, ağciyərin qeyri-adi auskultasiyası (eqofoniya, pıçıltı pektorofoniyası, xırıltılar və ya quru xartıltı) və ya taxikardiya daxildir. Vizuallaşdırma, torasentez, oksigenləşdirmə və Qram yaxmasında əldə edilən məlumat optimallaşdırılmalıdır.
XDP/ventilyasiya əlaqəli pnevmoniya (VƏP) üçün ciddi şübhənin olması yaxşıdır, beləki düzgün müalicə nə qədər tez başlasa ölüm göstəricisi bir o qədər az olar. Mikrobəleyhinə preparatların başlaması və həftələr ərzində davam etməsinin qarşısını almaq cəhdi olaraq düzgün və qısa mikrobəleyhinə terapiya təmin etmək üçün kliniki Ağciyər İnfeksiya Dərəcəsi (KAİD) [52] yaradılıb. VƏP diaqnozu qoyarkən KAİD-i kliniki kriteriya ilə istifadə etmənin, sadəcə kliniki kriteriyadan istifadə etmə dəqiqliklərini qarşılaşdırmaq barədə məlumat azdır; bunun üçün onun istifadəsi yenidən nəzərə alınmalıdır.
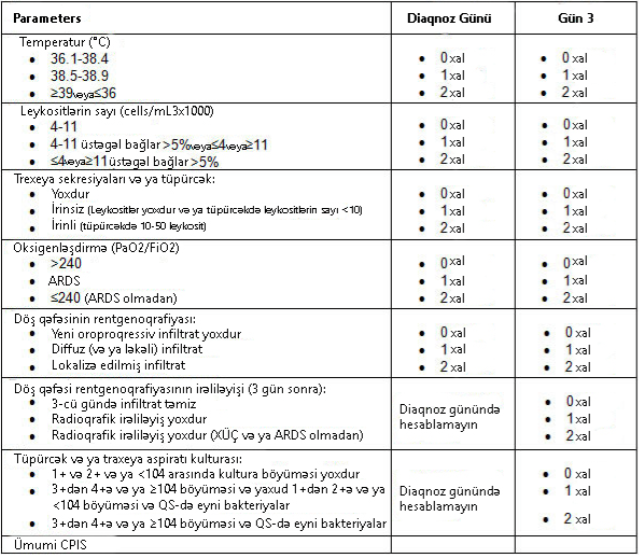
Cədvəl. KAİD qiymətləndirmə sistemi.
Anamnez və kliniki müayinə
Anamnezdə xəstənin əksər dərmana davamlı (DDP) patogenlərinin səbəb olduğu pnevmoniya riski olub-olmaması dəqiqləşdirilməlidir (məs. Psevdomonas aeruginosa, Klebsiella pnevmoniyae və MRSA). Bunu müəyyənləşdirmək əhəmiyyətlidir, çünki empirik antibiotik seçiminə təsir edir. DDP pnevmoniya üçün risk faktorları aşağıdakılardır:
- Əvvəlki 90 gündə mikrobəleyhinə müalicə
- VƏP vaxtı septik şok
- VƏP-dan əvvəl kəskin respirator sindromu
- 5 və ya daha çox müddətə xəstəxanaya yeləşdirilmək
- VƏP başlamazdan əvvəl kəskin böyrək köçürmə terapiyası.
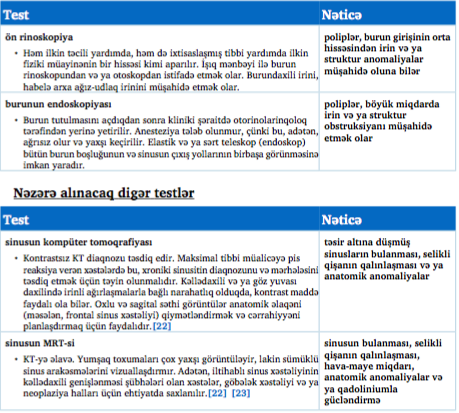
Döş qəfəsinin rentgenoqrafiyası və diaqnostik torakosentez
Döş qəfəsi ocaqlı vəya diffuz kölgəlik göstərir, bu diaqnoz üçün lazımdır. Döş qəfəsinin rentgenoqrafiyası, adətən, istər xəstəxana palatasında və ya İTŞ-də olan bütün xəstələr üçün keçirilir. Yan tərəfdən ön və arxa təsvirə üstünlük verilir. Kompüter tomoqrafiyası, xüsusilə radioqrafın keyfiyyəti pisdirsə və ya aydın olmayan kölgəlik varsa, lazım ola bilər. [Fig-1] [Fig-2] [Fig-3] [Fig-4]
Əgər döş qəfəsinin rentgenoqrafiyasında plevral maye görünürsə, və miqdarı minimaldan çoxdursa, diaqnostik torasentez edilməlidir. Plevral mayedən analizlər göstərir ki, plevral boşluq qurudulmalıdır pH <7.20, qlükoza səviyyəsi <2.2 mmol/L (<40 mq/dL), və LDH səviyyəsi >1000 U/L.
Oksigenləşdirmə vəziyyəti
Oksigenləşdirmə vəziyyətini müəyyənləşdirmək üçün əsas üsul ABG vasitəsi ilədir. Xüsusilə vaskulyarizasiya periferik olaraq sıxılıbsa, XDP əlamət və simptomları varsa, periferik sahədən alınan oksigen saturasiyası, səhvən, düzgün oksigenləşdirmənin olduğunu göstərə bilər. Xəstə yüksək FiO2 qəbul etməzdən əvvəl ABG çəkmək oksigenləşdirmə vəziyyəti haqqında daha dəqiq məlumat verir, lakin heç bir qeyri-stabil xəstədə artmış oksigen dayandırılmamalıdır.
Qram yaxması
Qram yaxması traxeya aspiratından, bronxoalveolyar lavaj (BAL) nümunəsindən və ya qorunan fırça nümunəsindən əldə edilə bilər. [53] Yaxmanı həmçinin tüpürcəkdən toplamaq mümkündür, lakin adı çəkilən tənəffüs yolları nümunələrinə üstünlük verilir. [8] Əgər bronxoskopiya planlaşdırıbsa və prosedura başlamazdan əvvəl patogenlərin kulturada böyüməsinin qarşısını alan mikrobəleyhinə preparatlar labüddürsə, kultura üçün sovurma üsulu ilə endotraxeya nümunəsi (qeyri-bronxoskopik BAL) və ya tüpürcək toplanmalıdır. Bəzi dəlillər endotraxeya aspirat əsaslı müalicənin BAL nümunələrinə əsasən aparılan müalicə ilə bənzər nəticələr verdiyini göstərir. [54]
Qan analizləri
Təkcə leykosit miqdarından istifadə edərək heç bir infeksion diaqnoz qoyulmamalıdır, lakin artmış leykosit miqdarı, yüksək qranulositoz və rabitələrin nisbəti döş qəfəsinin rentgenoqrafiyasında kölgəlik və digər əlamət və simptomlarla birgə nəzərə alındıqda XDP ilə əlaqəlidir. Leykopeniya daha ağır xəstəlik və hətta sepsisə işarə edə bilər.
İnfeksiya və sepsis biomarkerlərinin, C-reaktiv zülal və prokalsitonin qiymətləndirilib. VƏP olan və olmayan xəstələr arasında C-reaktiv zülal çox fərqli deyil. [55]
RİSK FAKTORLARI.
Ciddi risk faktorlar.
Zəif infeksiya nəzarəti/əl gigiyenası
• XDP-a səbəb olan patogenlər, o cümlədən Asinetobakter baumanni, xəstələrə tibb işçilərinin əllərindən ötürülür.
İntubasiya və mexaniki ventilyasiya; endotraxeya başlıq təzyiqi <20 sm H2O
• Alveollarda bakteriyaların ən yayılmış yoluxması orofaringeal patogenlərin mikroaspirasiyası və ya endotraxeyal boru başlığında bakteriya olan sekresiyaların sızması yolu ilədir. [18]
• XDP üçün patogen mənbələrinə tibbi cihazlar (endotraxeal borusunda yoluxmuş biotəbəqə), ətraf mühit (hava, su, avadanlıq), habelə mikroorqanizmlərin xəstədən xəstəyə tibb işçiləri vasitəsi ilə ötürülməsi daxildir.[21] [22]
• İntubasiya edilmiş xəstələrdə ventilyasiya əsaslı pnevmoniya (VƏP) nisbəti hər 1000 xəstədə 6-20 nəfərdir. Bu, xəstəxanaya yerləşdirilmiş hər 1000 xəstədə 5 -10 nəfər olan XDP nisbətindən daha çoxdur. Burun-traxeya intubasiyası edilmiş xəstələr ağız-traxeya intubasiyası edilənlərdən daha böyük risk altındadırlar.
Zəif risk faktorlar.
Yataq başlığı <30° bucaqda
• Mexaniki ventilyasiyalı xəstələrdə, radioaktiv nişanlı bağırsaq qidalanmasından istifadə edən tədqiqatlara əsasən, tam horizontal vəziyyətdə arxası üstə vəziyyət aspirasiyaya kömək edir. [25] Digər bir tədqiqata görə yarı-uzanmış xəstələrdə ventilyasiya əsaslı pnevmoniyanın (VƏP) nisbəti düz yatanlara nisbətən ciddi azaldılıb. [26] Bunun üçün də Amerika Torakal Cəmiyyəti, Amerika İnfeksion Xəstəliklər Cəmiyyəti və Xəstəliklərə Nəzarət və Profilaktika Mərkəzi tərəfindən yataq başlığını qaldırmaq tövsiyyə edilir və bu praktikanı dəstəkləyən dəlil az olsa da, əksər mütəxəssislər tərəfindən bəyənilir.[27] Daha keyfiyyətli dəlil toplamaq üçün səylər davam etdirilir.
H2 antaqonist və antasid istifadəsi
• Stress mənşəli xoranın profilaktikasında H2 antaqonist və ya antasidlərə nəzərən sukralfat istifadəsi haqqında ziddiyyətli tədqiqatlar var, ancaq sukralfat istifadə edərkən daha az ventilyasiya əlaqəli pnevmoniyaya (VƏP) yönəlmiş bir meyillilik var. Meta-analiz nəticəsində sukralfatın H2 və ya antasidlər qədər xoraların qarşısını aldığı müəyyənləşdirilib. [28] Geniş kontingentli bir tədqiqata görə H2 antaqonistləri mexaniki ventilyasiya edilən xəstələrdə proton nasos inhibitorlarından daha az pnevmoniya riski ilə əlaqəlidir. [29]
Pis ağız boşluğu gigiyenası
• Oral gigiyena praktikası CDC tərəfindən tövsiyyə edilir və oral gigiyenanın XDP-ı azaltdığını göstərən tədqiqatlara əsaslanır. [3] [30] [31] 11 potensial tədqiqat üzərində aparılan meta-analiz bu tədqiqatların üsullarında bir neçə problemi müzakirə edib. [32] Oral gigiyenanın müvəffəqiyyətinin böyük bir hissəsi koronar şuntlama əməliyyatı olan xəstələrdə qeydə alınıb. [33]
Sedativlərə fasilə verilməməsi
• Sedativlərin dayandırılması intubasiya müddətini qısaldır və bunun üçün də ventilyasiya əsaslı pnevmoniyanı (VƏP) azaldır. [34] [35] Sedativ fasilə verilməsi üçün daha çox İTŞ işçiləri tələb olunur və bu təcrübəni protokollara əlavə etməzdən əvvəl resursların mövcudluğu yoxlanılmalıdır.
DİAQNOSTİK TESTLƏR.
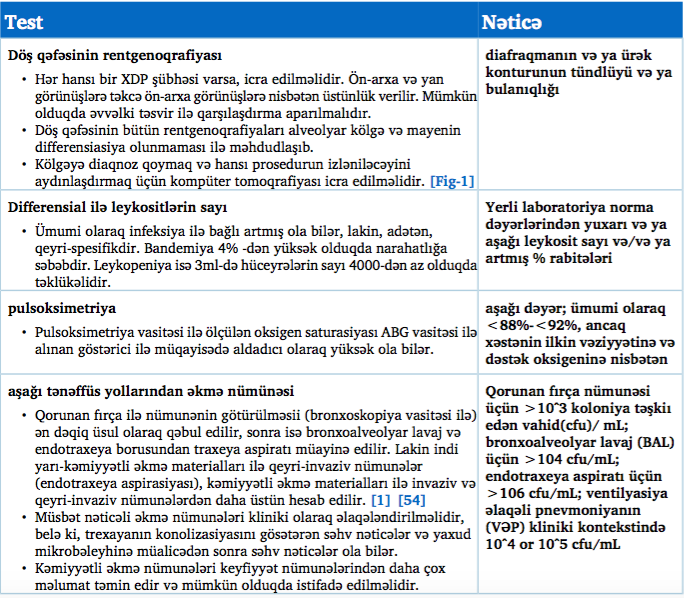
NƏZƏRƏ ALINMALI DİGƏR TESTLƏR.

Diaqnostik meyarlar
Xəstəxanadaxili pnevmoniya və ventilyasiya əlaqəli pnevmoniyalı böyüklərin idarə edilməsi: Amerika İnfeksion Xəstəliklər Cəmiyyəti və Amerika Torakal Cəmiyyətinin 2016 kliniki təcrübətəlimatları [1]
XDP diaqnozu müsbət vizuallaşdırma üsulu və 3 kliniki xüsusiyyətlərdən 2-ni tələb edir: hərarət >38°C (100.4°F), leykositoz və ya leykopeniya və yaxud irinli ifrazatlar.
MƏRHƏLƏLİ MÜALİCƏNİN ƏSASLARI.
Sürətli, düzgün və müvafiq antibiotik terapiyası XDP müalicəsi üçün əhəmiyyətlidir. Müalicə rejimləri əksər dərmana davamlı (DDP) patogenlər üçün risk faktorlarının olmasından asılıdır. Bu risk faktorları aşağıdakılardır: [8]
• Əvvəlki 90 gün ərzində olan antibiotik terapiyası
• Ventilyasiya əlaqəli pnevmoniya (VƏP) vaxtı septiki şok
• VƏP-dan əvvəl kəskin respirator sindrom
• 5 gün və ya daha çox müddətə xəstəxanaya yeləşdirilmək
• VƏP başlamazdan əvvəl kəskin böyrək köçürmə terapiyası.
Əgər yuxarıdakı risk faktorları varsa, geniş spektrli antibiotiklərlə birgə müalicə nəzərə alınır.[61]
Xəstəxana şəraitində hər hansı bir antibiotiklərin istifadəsi düşünülmüş olmalıdır, belə ki, bu, xüsusilə İTŞ-də rezistent ştammların inkişafına təsir edə bilər. DDP alovlanmaları, qram-mənfi patogenlərə qarşı beta-laktam və ya xinolonların həddən artıq istifadəsi zamanı baş verir. [62] Ümumiyyətlə, əgər hər hansı bir mikrobəleyhinə preparatın istifadəsinə üstünlük verilirsə, rezistentlik də baş verə bilər. Bir tədqiqatda, karbapanem (20) və kolistimetan(13) antibiotiklərindən uzun müddətli istifadədən sonra alovlanma baş verməsi haqqında məlumat verilir.[63]
Yeni XDP diaqnozu qoyulmuş xəstələrdə əvvəlcədən müəyyənləşdirilmiş antibiotik protokolu lazım deyil, ancaq xüsusilə həkimlərin ölüm göstəricisini azaltmaq imkanı olduğu müalicənin ilkin mərhələlərində xəstələrə düzgün müalicə verilməsi üçün tövsiyyə edilir. [2] [52] Protokolda seçiləcək olan dərman preparatlarının siyahısı və rezistentliyin artması halında dəyişdirilməsi mümkün olan rejim göstərilməlidir.[8] [52]
Empirik antibiotik terapiyası
Empirik antibiotik rejimləri həmişə yerli müqavimət şablonlarına uyğunlaşdırılmalıdır; antibioqramma hazırlanmalıdır. [61]
Əgər xəstədə DDP patogenləri üçün risk faktoru yoxdursa, pnevmoniyanın səbəbkar patogeni böyük ehtimalla Streptokokk pnevmoniyae, Hemofilus influenzae, metisillinə-həssas Stafilokokk aureus (MSSA) və ya antibiotikə-həssas enterik qram-mənfi bakteriyalardır (məs. Escherichia koli, Klebsiella pnevmoniyae, Enterobakter növlər, Proteus növləri və yaxud Serratia marsesens). Terapiyaya Psevdomonas aeruginosa üçün əhatə sahəsi olan monoterapiya daxildir: sefepim, seftazidim, imipenem/silastatin, meropenem, levofloksasin və ya piperasillin/tazobaktam.[1] [64] [65] Nəzərə alın ki, aminoglikozidlər bu siyahıda yoxdur, çünki onların XDP/VƏP səbəb olan P aeruginosa üçün əhatə sahəsinə baxmayaraq, risklərinin faydasından çox olduğu müşahidə edilib.[66]
Əgər xəstədə DDP patogenləri üçün risk faktorları yoxdursa, səbəbkar patogen böyük ehtimalla P aeruginosa, K pnevmoniyae (geniş spektrli beta-laktamaz [ESBL] ştammı), Asinetobakter növləri, MRSA və ya Legionella pnevmofiladır. Bu patogenlərin hər hansı birinə görə baş verən XDP/ventilyasiya əlaqəli pnevmoniya (VƏP) artan ölüm göstəricisi ilə əlaqələndirilir. [67] P aeruginosa risk faktorlarına yüksək keyfiyyətli Qram yaxması, qram-mənfi bakteriya və strukturlu ağciyər xəstəliyi daxildir. Əgər bu faktorlardan hər hansı biri mövcuddursa, və ya əgər xəstə mexaniki olaraq intubasiya və ventilyasiya edilirsə, və yaxud septik şok varsa, P aeruginosa üçün birləşdirilmiş terapiya təyin edilməlidir. DDP patogenlərinin olması ehtimalı çox olan xəstələr üçün birləşdirilmiş terapiyaya sefalosporin (məs. sefepim, seftazidim), karbapenem (məs. imipenem/silastatin, meropenem), beta-laktam/beta-laktamaz inhibitoru (məs. piperasillin/tazobaktam), və ya monobaktam (məs. aztreonam); əlavə olaraq xinolon (məs. siprofloksasin, levofloksasin) və ya aminoglikozid (məs. amikasin, gentamisin, tobramisin); əlavə olaraq linezolid və ya vancomisin (və ya alternativ olaraq telavansin) daxildir.[8]
Əgər Psevdomonasın səbəbkar patogen olması şübhəsi varsa, 2 antibiotik müxtəlif hərəkət rejimlərində empirik olaraq istifadə edilməlidir, rejimlərə müxtəlif psevdomona əleyhinə beta-laktamlar, karbapenemlər, xinolonlar və aminoqlikozidlər daxildir. IImipenem/silastatin və ya meropenem (karbapenem antibiotikləri) istifadə edilə bilər ancaq ertapenem istifadə olunmamalıdır, çünki P aeruginosanı əhatə etmir və ancaq xəstəxanadankənar pnevmoniya üçün təsdiqlənib Aminoqlikozidlər qram-mənfi bakteriyaları sürətlə öldürür, ancaq böyrək toksikliyi və ya ototoksikliyə səbəb ola bilər. Tobramisin gentamisinə nisbətən ağciyərə təsir baxımından nisbətən yaxşıdır və yeni müalicə üsulu olmasına baxmayaraq, nəfəsə çəkmə şəklində verilə bilər. Xinolonlar təsirlidir və siprofloksasinin nisbətən dar spektri var, lakin Psevdomonasa müqavimət hər il artır. Xinolonlar həm də Klostridium diffisil koliti ilə əlaqələndirilir. Həm aminoqlikozidlər və xinolonlar konsentrasiya əsaslı mikrobəleyhinə preparatlardır və qeyri-müntəzəm və yüksək dozalarla bu xüsusiyyətdən faydalanmaq üçün doza verilir, dərman səviyyələrini minimal inhibitor konsentrasiyasından (MIC) artıq olması üçün dozlaşdırılan vaxt əsaslı mikrobəleyhinə preparatlar (məs. beta-laktamlar) istisna edilir. Bu kontekstdə, tigesiklini imipenem/silastatinlə qarşılaşdıran bir tədqiqatda XDP xəstələrində qeyri-aşağı ancaq VƏP xəstələrində aşağı olduğu müşahidə edilib. [68] Nəticə etibarı ilə rejimlər lokal antibioqrammalara əsaslanmalıdır.
Əgər xəstədə MRSA infeksiya riski varsa, vankomisin və ya linezolid əlavə edilməlidir (məs. xəstə 3 antibiotik qəbul edəcək). MRSA üçün risk faktorlarına əvvəlki günlərdə mikrobəleyhinə preparatların istifadəsi, Stafilokokk aureus kulturalarının >20% MRSA müsbət (və ya bilinməyən faizli) olan İTŞ-yə müraciət və yüksək ölüm göstəricisi riski olması daxildir. Məlumata görə, linezolid və vankomisinin bənzər təsirdədirlər. Növbəti yoxlama məlumatları birmənalı deyil, və linezolid və vankomisinin bərabər olması və yaxud linezolidin daha effektiv olmasını göstərir. [69] [70]
Əgər xəstə başqa bir infeksiyadan ötrü antibiotiklər qəbul edərkən və ya daha sonra XDP diaqnozu qoyularsa, empirik müalicə fərqli sinifdən dərman preparatlarını daxil etməlidir. [8]
Patogen əsaslı antibiotik terapiyası
Kulturalar hazır olduqda sonra antibiotiklər müvafiq olaraq zəiflədilməlidir: müalicə hansı patogenin böyüdüyünə dair həssaslığa əsasən daraldılmalıdır və ya nəyin cücərmədiyindən asılı olaraq mikrobəleyhinə dərmanlar dayandırılmalıdır. Məsələn, əgər MRSA kulturası cücəribsə, linezolid davam etməli, etməyibsə dayandırılmalıdır.[76]
Təsdiqlənmiş qram-mənfi infeksiyanın müalicəsi üçün istifad edilən antibiotiklərin nümunələri (məs. Psevdomonas, Asinetobakter, Klebsiella, Serratia) sephalosporin (sefepim, seftazidim) və ya karbapenem (imipenem/silastatin, meropenem) və yaxud beta-laktamaz inhibitor (piperasillin/tazobaktam) və ya xinolon (siprofloksacin, levofloksasin) və yaxud aminoqlikozid (amikasin, gentamisin, tobramisin) və ya polimiksindir (kolistimetat). Tək antibiotiklə monoterapiya kifayət edəcək. Lakin əgər infeksiya müdaxil edilməsi çətin bir sahədədirsə, o cümlədən ağciyər absesi, empiyema və ya müşayiətçi endokarditdədirsə, kombinasiya halında 2 dərman preparatları istifadə edilə bilər. Kombinasiya rejimləri sefalosporin (sefepim, seftazidim), karbapenem (imipenem/silastatin, meropenem) və ya beta-laktamaz inhibitoru (piperasillin/tazobaktam), əlavə olaraq xinolon (siprofloksasin, levofloksasin) aminoqlikozid (amikasin, gentamisin, tobramisin) və ya polimiksin (kolistimetat) ibarət olmalıdır.
Ənənəvi olaraq hər hansı psevdomonal infeksiya 2 antibiotiklə müalicə edilib. 1989-da aparılan bir tədqiqatda Psevdomonas bakteremiya xəstələri, o cümlədən pnevmoniyalı xəstələr qiymətləndirilib və kombinasiya müalicəsi olanlar arasında daha aşağı ölüm göstəricisi olduğu müşahidə edilib.[75] O vaxtdan bəri tədqiqatlar tək və ya kombinasiya terapiyası keçən XDP xəstələri arasında nəticələrin bənzər olduğunu göstərib.[78] [79] [80] 3[C]Evidence Monoterapiyanın faydalarında daha az istənməyən hallar, daha az müqavimət və daha az xərc olur.
XDP-ın ən yayılmış səbəbi olan qram-müsbət patogen nümunəsi S aureusdur. Metisillinə-həssas ştammlar penisillin və ya sefalosporin ilə müalicə edilir. Əgər xəstənin penisillinlərə qarşı allergiyası varsa, linezolid və ya vankomisin istifadə edilə bilər. Metisillinə davamlı ştammlar linezolid və ya vankomisinlə müalicə edilir.
Əgər ESBL istehsal edən Enterobakteriyalar XDP-a səbəb olursa, onda tövsiyyə edilən birinci sıra müalicəsi karbanapem antibiotikidir. İkinci cərgə müalicəsi xinolonlardır. Hətta əgər patogenlər həssas olsa belə sefalosporinlər tövsiyyə edilmir, çünki başladıqdan sonra sürətli müqavimət təhlükəsi var. XDP-ın nadir müşahidə edilən səbəbi L pnevmofiladır. Müalicə ya xinolon, ya da makrolidlə aparıla bilər.
Terapiyanın davametmə müddəti
Hansı müalicənin tənzimlənəcəyi, hətta dayandırılacağı barədə qərar verməyə kömək edən üsullar kliniki Ağciyər İnfeksiyası Dərəcə (CPIS) əsasında hazırlanıb.[52] Diaqnoz günündə CPIS 5 kliniki xüsusiyyətin qiymətləndirilməsi vasitəsi ilə hesablanır, kriteriyanın şiddətinə görə hər xüsusiyyətə sıfırdan 2-yə qədər bir xal verilir (daha pis olduqda daha yüksək):
- Temperatur
- Leykositlərin sayı
- Oksigenləşdirmə
- Ağciyər radioqrafiyası
Daha sonra üçüncü gündə cəm yenidən hesablanır və 2 yeni kriteriya əlavə edilir:
- Ağciyər infiltratın irəliləyişi • Mikrobioloji məlumat.
Əgər hər iki gündə CPIS <6 olarsa, diaqnoz şübhəsi olan gündə başladılan mikrobəleyhinə preparatları dayandırmaq olar, çünki xəstənin immun sistemi ciddi surətdə zəifləmir və onda sepsis yoxdur. Bu 'qısa müddətli tepariya' adlanır. Əgər bu günlərin hər hansı birində CPIS 6 və ya daha yüksəkdirsə, antibiotiklər tam kurs boyunca davam etdirilməlidirlər.
Dəqiqlik tədqiqatlarından toplanan məlumat VƏP təsdiqləmək və ya çıxarmaq, və yaxud mikrobəleyhinə müalicənin davametmə müddətini təyin etmək üçün CPIS istifadəsini dəyərsizləşdirən zəif dəlillər göstərib.[1] [81]
Əgər xəstə kliniki və radioloji olaraq sabitdirsə, o cümlədən laboratoriya dəyərləri stabildirsə və Asinetobakter və ya P aeruginosa ilə yoluxmayıbsa, antibiotik terapiyasının davametmə müddəti 7 gündə qurtara bilər.[1] [64] [82] Baxmayaraq ki çox istifadə edilir, MRSA üçün daha uzunmüddətli terapiyanı dəstəkləyici məlumat yoxdur; əgər bakteremiya varsa 2 həftə və əgər XDP/VƏP empiyema və ya endokardit kimi ağırlaşma ilə əlaqəlidirsə, daha uzun vaxt verilməlidir. 7 ilə 8 gün arasında mikrobəleyhinə preparatlar qəbul edən xəstələrdə MDR patogenlərindən ötrü daha az təkrarlanan VƏP olur, ölüm göstəricisi, xəstəxanada qalma müddəti, müalicə uğursuzluğu və mexaniki intubasiya və ventilyasiya müddətlərində fərq olmur.[83] [84] XDP müalicəsində tarixən tətbiq edilən üsul olan daha uzun sürən antibiotik istifadəsinin əskinə ABŞ Xəstəliklərə Nəzarət və Profilaktika Mərkəzlərinin (CDC) stasionar xəstə şəraitində mikrobəleyhinə preparatların istifadəsinə istiqamətlənmiş optimallaşdırma kampaniyası uyğun olduqda mikrobəleyhinə dərmanlarla müalicənin dayandırılmasına yönəlib.[85] Nəticə olaraq əksək XDP müalicə müddətləri daha qısa ola bilər, lakin Psevdomonas və ya Asinetobakterin səbəb olduğu XDP yenə də 2 həftə müddətində müalicə edilməlidir.[82]
Əgər bu müddət ərzində heç bir yaxşılaşma müşahidə edilməzsə, davamlı və ya qeyri-adi (məs. göbələk mənşəli) patogenlərin antibiotik rejiminin dəyişdirilməsi nəzərə alınmalıdır. lakin xəstəni digər ağciyər xəstəliklərinə qarşı, o cümlədən effuziyanın ekssudat (məs. empiyema) və ya transudat olmasını aşkarlamaq üçün qiymətləndirmək də vacibdir.[8] Həmçinin infeksiyanın başqa qeyri-ağciyər mənbələri üçün də dəyərləndirmək vacibdir. Əvvəlcə nəzərə alınmayan müəyyən bir prosedura işarə edilməsi mümkündür, məsələn septik tromboflebit ehtimalını aradan çıxarmaq üçün venadaxili xətt ilə bir ətrafın ultrasəs müayinəsi. Bronxoskopiya və ya torakosentez də təkrarlana bilər. Ümumiyyətlə, müalicənin uğursuzluğuna aşağıdakılar səbəb ola bilər:[86]
- Ağırlaşma
- Səhv diaqnoz
- Səhv patogenin müalicəsi.
Təzyiq dəstəyinə ventilyasiya parametlərini dəyişmək və ya ossilyator rejimindnə istifadə etmək kimi strategiyalar tənəffüs yolları həkimi tərəfindən nəzərə alına bilər.
Müalicəyə cavab: CRP və prokalsitonin
Diaqnoz günündən başlayaraq dəyərlər meyilliliyini izləmək üçün prokalsitonin istifadə edilə bilər.[58] Bu məlumat mikrobəleyhinə preparatların nə vaxt dayandırılacağını təyin etmək üçün istifadə edilə bilər.[1]
YENİ TƏKLİF EDİLƏN VƏ TƏCRÜBƏDƏN KEÇİRİLƏN MÜALİCƏ ÜSULLARI.
- Aerozollaşdırılmış antibiotik terapiyası
İnhalyasiyon antibiotiklərin istifadəsinə dair yeni məlumatlar mövcuddur. Bir potensial, plasebo ilə idarə edilən tədqiqatda respirator əlamətlərin aerozollaşdırılmış antibiotiklərin istifadəsi ilə azalması aşkarlanmışdır.[90] 7 kiçik tədqiqatın meta analizi göstərmişdir ki, aerozollaşdırılmış antibiotiklərlə monoterapiya, ümumi adi terapiyadan geri qalmır.[91] Ancaq venadaxili terapiya mümkün olmadıqda belə terapiya tövsiyyə edilir. İnfeksion Xəstəliklər Əczaçılığı Cəmiyyəti (İXƏC) tərəfindən nəşr edilən bir icmalda, dəlil əsaslı tövsiyyələr, o cümlədən XDP üçün bir neçə antibiotik dozalama təklif edir.[92] İcmala görə ən yaxşı namizədlər venadaxili antibiotiklərə reaksiya verməyən, təkrarlanan XDP-ları olan və yaxud DDP-lərə görə XDP olanlardır. XDP/VƏP üçün 2016-cı il təlimatları, ancaq aminoqlikozid və ya polimiksinlərə həssas olan patogenə yoluxmuş xəstələrə inhalyasiyon mikrobəleyhinə preparatlar tövsiyyə edir. [1] Bu əhalidə mənfi tədqiqatlar mövcuddur. [93]
Iklaprim, DDP -lərə qarşı yeni mikrobəleyhinə preparpatların yayılmasını sürətləndirmək üçün sentyabr 2015-ci il tarixdə, ABŞ Qida və Dərman Administrasiyası (QDA) tərəfindən sürətli statusa təqdim edilən 3-cü mərhələ sınaq preparatıdır. . Iklaprimin müxtəlif rezistent patogenlərə, o cümlədən MRSA və əksər dərmana davamlı Streptokokk pnevmoniyae qarşı geniş spektrli təsiri var. Dərman XDP və dəri struktur infeksiyalarına qarşı təsirlidir. İklaprim bakterial dihidrofolat reduktaz inhibitorudur. 70 xəstəxanadaxili pnevmoniyalı xəstə üzərində aparılan tədqiqat iklaprim və vankomisin arasında kliniki sağalma göstəricisini müqayisə etmişdir İklaprimdə sağalma göstəricisi 74% və 63%, vankomisində sağalma göstəricisi 52%-dir. [94] Tədqiqat əlavə doza olmadan,sabit vankomisin dozası ilə məhdudlaşdırılmışdı.
- Yeni antibiotik terapiyası
Seftobiprol, beşinci nəsil sefalosporin Avropada XDP və xəstəxanadankənar pnevmoniyanın (XKP) müalicəsi üçün təsdiqlənib. O MRSA və qram-mənfi bakteriyalara, o cümlədən Psevdomonas aeruginosaya qarşı təsirlidir. Digər bir beşinci nəsil sefalosporin, seftarolin (MRSA qarşı təsiri təmin edən) XKP üçün təsdiqlənib, lakin XDP üçün təsdiqlənməyib. İki son təsdiqlənmiş geniş spektrli mikrobəleyhinə preparatlar, seftazidim/avibaktam və seftolozan/tazobaktam XDP və ya VƏP (ventilyasiya əlaqəli pnevmoniya) xaricində infeksiyalar üçün nəzərdə tutulub. Seftazidim/avibaktamın genişləndirilmiş spektrli beta-laktamazlara (ESBL) qarşı təsiri var. Seftazidim/avibaktamın genişləndirilmiş spektrli beta-laktamazlara (ESBL) qarşı təsiri var. Profilaktik antibiotiklərin istifadəsi əks göstərişdir. Bir tədqiqata görə venadaxili profilaktik antibiotiklər qəbul edən xəstələr arasında daha aşağı XDP olduğu göstərilir, [95] digər tədqiqatlar isə belə xəstələrin daha sonra infeksiyalara aparan DDP-lər ilə kolonizasiya edildiklərini göstərir.[96] [97] Seçilmiş xəstələrdə qısa müddətli profilaktik antibiotiklərdən istifadə etmək faydalı ola bilər. [8]
ABŞ QDA tərəfindən sürətli hazırlanmasına icazə verilən, pnevmoniyanın müalicəsi üçün 2 monoklon anticisimləri vardır. Birincisi P aeruginosa qarşı geniş reaktiv monoklon anticismidir (immunoqlobulin G). 1-ci mərhələ tədqiqatı 84 gün ərzində dərmanın üç fərqli dozası qiymətləndirilib. [98] Heç bir ciddi əks təsirləri aşkarlanmayıb və az əhəmiyyətli mənfi təsirlər dərmanla əlaqəli deyildir. İkinci monoklon anticismi AR-301, MRSA da daxil olmaqla Stafilokokk aureus, toksininə qarşı, G1 immunoqlobulinidir. Hazırda dərman preparatının təhlükəsizliyini və effektivliyini qiymətləndirən 2 -ci mərhələ tədqiqatı, müşahidəyə ən azı 52 xəstəni cəlb edib və iştirakçılar iki hissəyə bölünüb: mikrobəleyhinə dərmanlarla müalicə edilənlər və mikrobəleyhinə dərmanlar və immunoqlobulinlə müalicə edilənlər. Avropa İttifaqı AR-301-ə nadir xəstəliklər dərman preparatı təyinatı verib. Araşdırılan digər monoklon anticisimlərə P aeruginosaya qarşı lipopolisaxxarid, Asinetobakter növlərinə qarşı başqa lipopolisaxxarid və tənəffüs sinsitik virusuna qarşı başqa bir lipopolisaxxarid aiddir.
- Gümüş üzlüklü endotraxeya boruları
Gümüş üzlüklü endotraxeya boruları, boru üzündə olan patogenləri öldürür. Gümüşlə üzlənmiş boruların ən geniş tədqiqatı, gümüşlə üzlənmiş boru ilə ventilyasiya edilənlərdə daha az pnevmoniya olduğunu aşkarlayıb.[45] 1509 xəstənin buraxılmasına baxmayaraq, xəstəxanada qalma müddəti və ya ölüm göstəricisində fərqi aşkarlamaq üçün tədqiqat kifayət qədər davam etdirilməyib.
Mexaniki ventilyasiya edilən xəstələrdə erkən və gec traxeotomiya ,ventilyasiya əlaqəli pnevmoniyaların sayında və nəticələrində fərqin aşkarlanması məqsədi ilə tədqiq edilmiş, lakin əsaslı nəticələr əldə edilməmişdir.[99] [100]
- Steril mexaniki intubasiya
Tədqiqatların yeni sferasına , endotraxeal intubasiya zamanı sterilliyin rolu aiddir. Belə görünür ki, təcili yardım şöbəsində intubasiya edilən xəstələrdə daha yüksək VƏP riski var, ancaq əgər xəstələr ilkin olaraq təmiz və nəzarət altında olan mühitdə intubasiya edilməyibsə, onların yenidən intubasiya edilməsini tələb edən siyasəti dəstəkləyən kifayət qədər məlumat yoxdur. [101]
ABŞ-da aparılan təsadüfi, nəzarət edilən tədqiqatda xəstəxanaya yerləşdirilmiş xəstələrə gündə 2 dəfə 15 dəqiqəlik osteopatik manipulyasiya müalicəsi verilib (məs. torax giriş miofassial boşalma), və protokola uyğun əhali arasında, təsadüfi olan əhali istisna olmaqla,xəstəxanada qalma müddətində, venadaxili antibiotik müddətində və tənəffüs pozğunluğu və ya ölüm sayında ciddi azalma müşahidə edilib. [102]
VƏP xəstələrində probiotiklərin istifadəsi təsadüfi nəzarət sınaqlarının mövzusu olub; ancaq nəticələr əsaslı olmayıb. Bir tədqiqatda Synbiotic 2000 Forte (içərisində Pediokokk pentoseseus, Leykonostok mesenteroidlər, L parakasey ssp və L plantaru var) gündə iki dəfə plaseboya qarşı sınanıb.[103] VƏP hallarının baş vermə tezliyi qruplar arasında bənzər olduğu müşahidə edilib (müdaxilə qrupunda 9%, plasebo qrupunda 13%). Ventilyasiya günləri, İTŞ-də qalma müddəti və ölüm göstəricisi də bənzər idi. Digər bir tədqiqatdə gündə iki dəfə probiotik Laktobasillus rhamnosus plaseboya qarşı qiymətləndirilib. [104] VƏP baş vermə tezliyi probiotik qrupda ciddi surətdə daha az idi (19% qarşı 40%). VƏP yoluxmasl üçün daha uzun müddət, habelə patogen növlərlə daha az yoluxma göstərici də müşahidə edilib; ancaq mexaniki ventilyasiyanın müddəti, İTŞ-də qalma müddəti və ümumi xəstəxanada qalma müddəti qruplar arasında bənzər idi. 2012 -2013-cü ilərdə 19 tədqiqat və 3 meta-analiz aparılıb, hər icmalda tədqiqatlar birgə işlənilib. [105] [106] [107] Nəticələr ziddiyyətli idi. Gələcəkdə təqdiqatlar müəyyən bir əhali qrupunda, məsələn travma xəstələrində fayda aşkarlaya bilər. [107]
Makrolid antibiotiklərinin iltihabəleyhinə təsirlərinin tədqiqati digər xəstəlik növlərində aparılıb, buna ən yaxın olanı xəstəxanadankənar pnevmoniyadır. VƏP xəstələrini müalicə etmək üçün klaritromisindən istifadə edən , təsadüfi kliniki tədqiqat 3 günlük klaritromisin kursu keçən xəstələrdə daha yüksək iltihabəleyhinə sitokinlər olduğunu aşkarlayıb; ancaq ümumi nəticələr ölçülməyib. [108] Nəticələrə görə klaritromisinin tətbiq edilməsi pro-iltihabi və iltihabəleyhinə maddələr arasında tarazlığı bərpa edib.
BİBLİOQRAFİYA.
1. Kalil AC, Metersky ML, Klompas M, et al. Management of adults with hospital-acquired and ventilator-associated pneumonia: 2016 clinical practice guidelines by the Infectious Diseases Society of America and the American Thoracic Society. Clin Infect Dis. 2016;63:e61-e111. Tam mətn Abstrakt
2. Iregui M, Ward S, Sherman G, et al. Clinical importance of delays in the initiation of appropriate antibiotic treatment for ventilator-associated pneumonia. Chest. 2002;122:262-268. Tam mətn Abstrakt
3. Tablan OC, Anderson LJ, Besser R, et al. Guidelines for preventing health-care-associated pneumonia, 2003: recommendations of CDC and the Healthcare Infection Control Practices Advisory Committee. MMWR Recomm Rep. 2004;53:1-36. Tam mətn Abstrakt
4. Masterton RG, Galloway A, French G, et al. Guidelines for the management of hospital-acquired pneumonia in the UK: report of the working party on hospital-acquired pneumonia of the British Society for Antimicrobial Chemotherapy. J Antimicrob Chemother. 2008;62:5-34. Tam mətn Abstrakt
5. Richards MJ, Edwards JR, Culver DH, et al. Nosocomial infections in medical intensive care units in the United States: National Nosocomial Infections Surveillance System. Crit Care Med. 1999;27:887-892. Abstrakt
6. Muscedere JG, Day A, Heyland DK. Mortality, attributable mortality, and clinical events as end points for clinical trials of ventilator-associated pneumonia and hospital-acquired pneumonia. Clin Infect Dis. 2010;51(suppl 1):S120-S125. Tam mətn Abstrakt
7. Kollef MH, Hamilton CW, Ernst FR. Economic impact of ventilator-associated pneumonia in a large matched cohort. Infect Control Hosp Epidemiol. 2012;33:250-256. Abstrakt
8. American Thoracic Society; Infectious Diseases Society of America. Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. Am J Respir Crit Care Med. 2005;171:388-416. Tam mətn Abstrakt
9. Melsen WG, Rovers MM, Koeman M, et al. Estimating the attributable mortality of ventilator-associated pneumonia from randomized prevention studies. Crit Care Med. 2011;39:2736-2742. Abstrakt
10. Heyland DK, Cook DJ, Griffith L, et al. The attributable morbidity and mortality of ventilator-associated pneumonia in the critically ill patient. Am J Respir Crit Care Med. 1999;159:1249-1256. Tam mətn Abstrakt
11. Mosier MJ, Pham TN. American Burn Association practice guidelines for prevention, diagnosis, and treatment of ventilator-associated pneumonia (VAP) in burn patients. J Burn Care Res. 2009;30:910-928. Abstrakt
12. Rubinstein E, Kollef MH, Nathwani D. Pneumonia caused by methicillin-resistant Staphylococcus aureus. Clin Infect Dis. 2008;46 Suppl 5:S378-S385. Abstrakt
13. Allen M, Mirsaeidi M, Peyrani P, et al. Emergence of community-associated MRSA as etiology of hospital-acquired pneumonia and ventilator-associated pneumonia: results from the IMPACT HAP study. Paper presented at: 46th Annual Meeting of ICAAC/IDSA; October 2008; Washington, D.C.
14. Sopena N, Sabrià M; Neunos 2000 Study Group. Multicenter study of hospital-acquired pneumonia in non-ICU patients. Chest. 2005;127:213-219. Tam mətn Abstrakt
15. el-Ebiary M, Sarmiento X, Torres A, et al. Prognostic factors of severe Legionella pneumonia requiring admission to ICU. Am J Respir Crit Care Med. 1997;156:1467-1472. Tam mətn Abstrakt
16. Wilde JA, McMillan JA, Serwint J, et al. Effectiveness of influenza vaccine in health care professionals: a randomized trial. JAMA. 1999;281:908-913. Tam mətn Abstrakt
17. Sarubbi FA Jr, Kopf HB, Wilson MB, et al. Increased recovery of Aspergillus flavus from respiratory specimens during hospital construction. Am Rev Respir Dis. 1982;125:33-38. Abstrakt
18. Cook D, De Jonghe B, Brochard L, et al. Influence of airway management on ventilator-associated pneumonia: evidence from randomized trials. JAMA. 1998;279:781-787. Abstrakt
19. Bergmans DC, Bonten MJ, van Tiel FH, et al. Cross-colonisation with Pseudomonas aeruginosa of patients in an intensive care unit. Thorax. 1998;53:1053-1058. Tam mətn Abstrakt
20. Craven DE, Steger KA. Nosocomial pneumonia in mechanically ventilated adult patients: epidemiology and prevention in 1996. Semin Respir Infect. 1996;11:32-53. Abstrakt
21. Pittet D, Hugonnet S, Harbarth S, et al. Effectiveness of a hospital-wide programme to improve compliance with hand hygiene. Lancet. 2000;356:1307-1312. Abstrakt
22. Kollef MH. The prevention of ventilator-associated pneumonia. N Engl J Med. 1999;340:627-634. Abstrakt
23. Cook D, Guyatt G, Marshall J, et al. A comparison of sucralfate and ranitidine for the prevention of upper gastrointestinal bleeding in patients requiring mechanical ventilation. N Engl J Med. 1998;338:791-797. Tam mətn Abstrakt
24. Donowitz GR, Mandell GL. Acute pneumonia. In: Mandell GL, Bennett JE, Dolin R, eds. Principles and practice of infectious diseases. 6th ed. Philadelphia, PA: Churchill Livingstone; 2005:819-845.
25. Hess DR. Patient positioning and ventilator-associated pneumonia. Respir Care. 2005;50:892-898. Abstrakt
26. Drakulovic MB, Torres A, Bauer TT, et al. Supine body position as a risk factor for nosocomial pneumonia
in mechanically ventilated patients: a randomised trial. Lancet. 1999;354:1851-1858. Abstrakt
27. Niël-Weise BS, Gastmeier P, Kola A, et al. An evidence-based recommendation on bed head elevation for
mechanically ventilated patients. Crit Care. 2011;15:R111. Tam mətn Abstrakt
28. Heyland DK, Drover JW, MacDonald S, et al. Effect of postpyloric feeding on gastroesophageal regurgitation and pulmonary microaspiration: results of a randomized controlled trial. Crit Care Med. 2001;29:1495-1501. Abstrakt
29. MacLaren R, Reynolds PM, Allen RR. Histamine-2 receptor antagonists vs proton pump inhibitors on gastrointestinal tract hemorrhage and infectious complications in the intensive care unit. JAMA Intern Med. 2014;174:564-574. Abstrakt
30. Schleder B, Stott K, Lloyd RC. The effect of a comprehensive oral care protocol on patients at risk for ventilator-associated pneumonia. Crit Care Nurse Clinic N Am. 2002;4:27-30.
31. Yoneyama T, Yoshida M, Ohrui T, et al. Oral care reduces pneumonia in older patients in nursing homes. J Am Geriatr Soc. 2002;50:430-433. Abstrakt
32. Berry AM, Davidson PM, Masters J, et al. Systematic literature review of oral hygiene practices for intensive care patients receiving mechanical ventilation. Am J Crit Care. 2007;16:552-562. Abstrakt
33. DeRiso AJ 2nd, Ladowski JS, Dillon TA, et al. Chlorhexidine gluconate 0.12% oral rinse reduces the incidence of total nosocomial respiratory infection and nonprophylactic systemic antibiotic use in patients undergoing heart surgery. Chest. 1996;109:1556-1561. Tam mətn Abstrakt
34. Marelich GP, Murin S, Battistella F, et al. Protocol weaning of mechanical ventilation in medical and surgical patients by respiratory care practitioners and nurses: effect on weaning time and incidence of ventilator-associated pneumonia. Chest. 2000;118:459-467. Tam mətn Abstrakt
35. Kress JP, Pohlman AS, O'Connor MF, et al. Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. N Engl J Med. 2000;342:1471-1477. Tam mətn Abstrakt
36. Allegranzi B, Pittet D. Preventing infections acquired during health-care delivery. Lancet. 2008;372:1719-1720. Abstrakt
37. Boyce JM, Pittet D. Guideline for hand hygiene in health-care settings: recommendations of the Healthcare Infection Control Practices Advisory Committee and the HICPAC/SHEA/APIC/IDSA Hand Hygiene Task Force. MMWR Recomm Rep. 2002;51:1-44. Tam mətn Abstrakt
38. Burns KE, Meade MO, Premji A, et al. Noninvasive positive-pressure ventilation as a weaning strategy for intubated adults with respiratory failure. Cochrane Database Syst Rev. 2013;(12):CD004127. Tam mətn Abstrakt
39. Muscedere J, Rewa O, McKechnie K, et al. Subglottic secretion drainage for the prevention of ventilator-associated pneumonia: a systematic review and meta-analysis. Crit Care Med. 2011;39:1985-1991. Abstrakt
40. Han JN, Liu YP, Ma S, et al. Effects of decreasing the frequency of ventilator circuit changes to every 7 days on the rate of ventilator-associated pneumonia in a Beijing hospital. Respir Care. 2001;46:891-896. Abstrakt
41. Han J, Liu Y. Effect of ventilator circuit changes on ventilator-associated pneumonia: a systematic review and meta-analysis. Respir Care. 2010;55:467-474. Tam mətn Abstrakt
42. Panchabhai TS, Dangayach NS, Krishnan A, et al. Oropharyngeal cleansing with 0.2% chlorhexidine for prevention of nosocomial pneumonia in critically ill patients: an open-label randomized trial with 0.01% potassium permanganate as control. Chest. 2009;135:1150-1156. Tam mətn Abstrakt
43. Klompas M, Speck K, Howell MD, et al. Reappraisal of routine oral care with chlorhexidine gluconate for patients receiving mechanical ventilation: systematic review and meta-analysis. JAMA Intern Med. 2014;174:751-761. Abstrakt
44. Alexiou VG, Ierodiakonou V, Dimopoulos G, et al. Impact of patient position on the incidence of ventilator-associated pneumonia: a meta-analysis of randomized controlled trials. J Crit Care. 2009;24:515-522. Abstrakt
45. Kollef MH, Afessa B, Anzueto A, et al. Silver-coated endotracheal tubes and incidence of ventilator-associated pneumonia: the NASCENT randomized trial. JAMA. 2008;300:805-813. Tam mətn Abstrakt
46. Damas P, Frippiat F, Ancion A, et al. Prevention of ventilator-associated pneumonia and ventilator-associated conditions: a randomized controlled trial with subglottic secretion suctioning. Crit Care Med. 2015;43:22-30. Abstrakt
47. Lacherade JC, De Jonghe B, Guezennec P, et al. Intermittent subglottic secretion drainage and ventilator-associated pneumonia: a multicenter trial. Am J Respir Crit Care Med. 2010;182:910-917. Tam mətn Abstrakt
48. Siempos II, Ntaidou TK, Falagas ME. Impact of the administration of probiotics on the incidence of ventilator-associated pneumonia: a meta-analysis of randomized controlled trials. Crit Care Med. 2010;38:954-962. Abstrakt
49. Canter RR, Harvey SE, Harrison DA, et al. Observational study of current use of selective decontamination of the digestive tract in UK Critical Care units. Br J Anaesth. 2014;113:610-617. Abstrakt
50. Huang JC, Cao Y, Liao C, et al. Effect of histamine-2-receptor antagonists versus sucralfate on stress ulcer prophylaxis in mechanically ventilated patients: a meta-analysis of 10 randomized controlled trials. Crit Care. 2010;14:R194. Tam mətn Abstrakt
51. van Zanten AR, Brinkman S, Arbous MS, et al. Guideline bundles adherence and mortality in severe sepsis and septic shock. Crit Care Med. 2014;42:1890-1898. Abstrakt
52. Singh N, Rogers P, Atwood CW, et al. Short-course empiric antibiotic therapy for patients with pulmonary infiltrates in the intensive care unit: a proposed solution for indiscriminate antibiotic prescription. Am J Respir Crit Care Med. 2000;162:505-511. Tam mətn Abstrakt
53. Torres A, Ewig S. Diagnosing ventilator-associated pneumonia. N Engl J Med. 2004;350:433-435. Abstrakt
54. Canadian Critical Care Trials Group. A randomized trial of diagnostic techniques for ventilator-associated
pneumonia. N Engl J Med. 2006;355:2619-2630. Tam mətn Abstrakt
55. Ramirez P, Garcia MA, Ferrer M, et al. Sequential measurements of procalcitonin levels in diagnosing
ventilator-associated pneumonia. Eur Respir J. 2008;31:356-362. Tam mətn Abstrakt
56. Sahn SA. Diagnosis and management of parapneumonic effusions and empyema. Clin Infect Dis.
2007;45:1480-1486. Tam mətn Abstrakt
57. Schuetz P, Briel M, Christ-Crain M, et al. Procalcitonin to guide initiation and duration of antibiotic treatment in acute respiratory infections: an individual patient data meta-analysis. Clin Infect Dis. 2012;55:651-662. Tam mətn Abstrakt
58. Seppä Y, Bloigu A, Honkanen PO, et al. Severity assessment of lower respiratory tract infection in elderly patients in primary care. Arch Intern Med. 2001;161:2709-2713. Tam mətn Abstrakt
59. Clec'h C, Timsit JF, De Lassence A, et al. Efficacy of adequate early antibiotic therapy in ventilator-associated pneumonia: influence of disease severity. Intensive Care Med. 2004;30:1327-1333. Abstrakt
60. Muscedere JG, Shorr AF, Jiang X, et al. The adequacy of timely empiric antibiotic therapy for ventilator-associated pneumonia: an important determinant of outcome. J Crit Care. 2012;27:322. Abstrakt
61. Ibrahim EH, Ward S, Sherman G, et al. Experience with a clinical guideline for the treatment of ventilator-associated pneumonia. Crit Care Med. 2001;29:1109-1115. Abstrakt
62. Manzur A, Tubau F, Pujol M, et al. Nosocomial outbreak due to extended-spectrum-beta-lactamase- producing Enterobacter cloacae in a cardiothoracic intensive care unit. J Clin Microbiol. 2007;45:2365-2369. Tam mətn Abstrakt
63. Mentzelopoulos SD, Pratikaki M, Platsouka E, et al. Prolonged use of carbapenems and colistin predisposes to ventilator-associated pneumonia by pandrug-resistant Pseudomonas aeruginosa. Intensive Care Med. 2007;33:1524-1532. Abstrakt
64. Franzetti F, Antonelli M, Bassetti M, et al. Consensus document on controversial issues for the treatment of hospital-associated pneumonia. Int J Infect Dis. 2010;14 Suppl 4:S55-S65. Abstrakt
65. Heyland DK, Dodek P, Muscedere J, et al. Randomized trial of combination versus monotherapy for the empiric treatment of suspected ventilator-associated pneumonia. Crit Care Med. 2008;36:737-744. Abstrakt
66. Kim JW, Chung J, Choi SH, et al. Early use of imipenem/cilastatin and vancomycin followed by de-escalation versus conventional antimicrobials without de-escalation for patients with hospital-acquired pneumonia in a medical ICU: a randomized clinical trial. Crit Care. 2012;16:R28. Tam mətn Abstrakt
67. Kett DH, Cano E, Quartin AA, et al. Implementation of guidelines for management of possible multidrug-resistant pneumonia in intensive care: an observational, multicentre cohort study. Lancet Infect Dis. 2011;11:181-189. Abstrakt